Xavier Trepat, profesor ICREA del IBEC y miembro fundador de España Salud Fundación “Controlar las fuerzas de las células permitiría frenarlas en la metástasis”
Si el siglo XX fue el de la Física, con sus grandes avances en las teorías sobre la materia inerte, el siglo XXI tiene puesto el foco en la Biología. Pero conceptos que proceden de la física también pueden contribuir a ensanchar el conocimiento de la materia viva. Sobre ellos se despliegan las líneas de investigación en el laboratorio de Xavier Trepat Guixer, profesor ICREA del Instituto de Bioingeniería de Catalunya (IBEC). Trepat también forma parte del consejo científico de España Salud Fundación.
Formado en Física e Ingeniería Electrónica en la Universidad de Barcelona, donde se doctoró en la Facultad de Medicina, Xavier Trepat dirige, tras su paso por la Universidad de Harvard, un equipo en el IBEC desde 2008, donde se integran de forma pionera aproximaciones de la física con la función biológica de las células. Sus trabajos han generado conocimiento en el campo de la mecanobiología y han permitido el desarrollo y la patente de varias tecnologías que miden las propiedades mecánicas celulares a escala micro y nanométrica. Por sus aportaciones ha merecido el Premio Fundación Lilly de Investigación Biomédica Preclínica, que recibió este año junto al neurólogo Xavier Montalban en la categoría de Investigación Biomédica Clínica. Este año también ha sido galardonado con el Rey Jaime I de Investigación Biomédica.
¿Cómo termina un físico investigando en la metástasis?. Cuando acabé mis estudios de física, me llamaron mucho la atención las ciencias de la vida. Me pareció que los grandes problemas de mi generación de investigadores estarían en entender cómo funcionan los seres vivos. La física tuvo un éxito enorme en el siglo XX entendiendo el funcionamiento de la materia inerte. El reto del siglo XXI es entender la materia viva, y para ello debemos integrar técnicas y conceptos de la física con los de la biología.
Sea como fuere, parece que ha elegido bien su carrera profesional: este año ha sido reconocido con el Premio de la Fundación Lilly y el Jaume I. ¿Cómo (o en qué) influyen los premios en el trabajo científico?. Siempre es bonito que reconozcan tu trabajo. Yo lo vivo como un reconocimiento a un campo de investigación al que nadie hacía caso hace unos años y ahora se ha establecido como uno de los que tiene más crecimiento a nivel mundial.
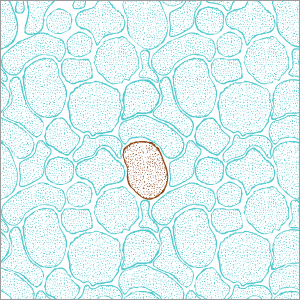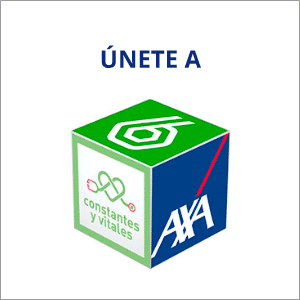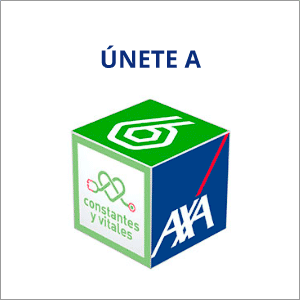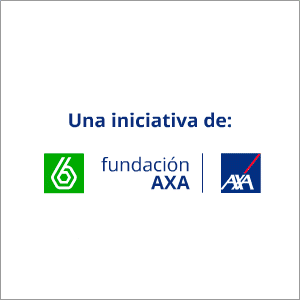
Centrándonos en las células tumorales, se sabe que crean la metástasis gracias a su capacidad para moverse. ¿Qué han hallado sobre ese movimiento?. Hemos entendido los diferentes mecanismos que propulsan las células en diferentes contextos. Las células tienen varias estrategias para moverse, y cuando bloqueas una, entonces utilizan otra. Es por ello, en parte, por lo que es tan difícil luchar contra la metástasis.
¿Y qué les gustaría averiguar?. Nos gustaría encontrar mecanismos para controlar las fuerzas que generan las células, y así poder acelerarlas o pararlas según nuestras necesidades.
Otra de sus líneas de investigación busca la manera de favorecer el movimiento de células inmunes para que accedan al tumor y lo eliminen. ¿Cómo lo harían?. En la mayoría de sólidos, las células inmunes no pueden penetrar en el tumor y matar las células cancerosas. Quedan atrapadas en el entorno tumoral que está compuesto de fibras y de unas células llamadas fibroblastos. Esta exclusión de las células inmunes es uno de los principales problemas para avanzar en la efectividad de las inmunoterapias. Cada vez más sabemos cómo conseguir que las células inmunes maten a las cancerosas, pero estos esfuerzos son en vano si no consiguen llegar al tumor. Intentamos desarrollar ensayos que nos permitan estudiar qué impide el movimiento de las células inmunes, ya sean causas físicas o bioquímicas.
¿En qué tumores específicos están investigando?. De momento nos centramos en cáncer de colon y de mama, pero el problema es general en tumores sólidos.
Cuando dos personas se dan un abrazo, hacen la fuerza de un newton, explica, y cuando dos células interaccionan entre ellas, la fuerza es de un nanonewton (mil millones de veces más pequeña que la de un abrazo). ¿Con qué tecnología miden ese ‘abrazo celular’? ¿Cómo esperan que se optimice ese tipo de tecnología, hacia dónde se dirige?. Sintetizamos geles muy blandos en forma de esfera y de un tamaño parecido al de las células. Entonces insertamos estas pequeñas esferas en los tejidos y las visualizamos con microscopía. Midiendo cómo se deforman estas esferas podemos calcular la fuerza que hacen las células. Queremos simplificar y estandarizar esta tecnología para que pueda ser usada por investigadores que no sean expertos en el campo.
Afirma que “intentar entender los organismos vivos sin considerar tanto la biología como la física es como intentar escribir un libro usando solo la mitad del alfabeto”. ¿Qué hallazgos en el campo de la medicina que se resisten ahora podrían escribirse con el alfabeto completo?. Muchísimos problemas. Por ejemplo, cómo se desarrollan los embriones. Hoy en día conocemos muchas de los procesos bioquímicos y genéticos asociados con el crecimiento de los embriones, pero solo con medidas de fuerzas podremos entender cómo consiguen adoptar las formas que dan lugar a los órganos. Del mismo modo, entender las fuerzas que generan las células nos permitirá entender mejor la metástasis y mejorar la regeneración de tejidos. Sonia Moreno (DM)