Evitar la herencia de una enfermedad
 El diagnóstico genético preimplantacional permite seleccionar embriones sin patología para transferirlos al útero materno
El diagnóstico genético preimplantacional permite seleccionar embriones sin patología para transferirlos al útero materno
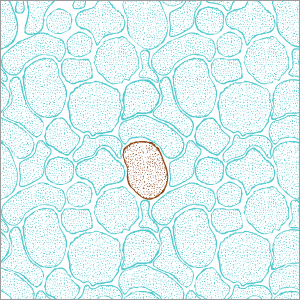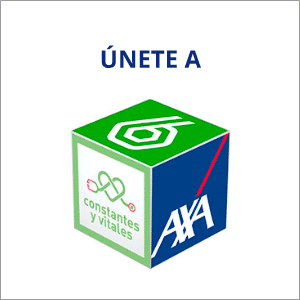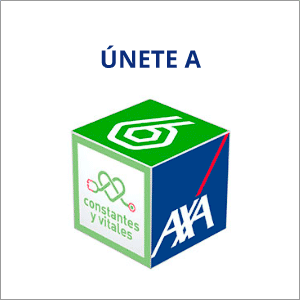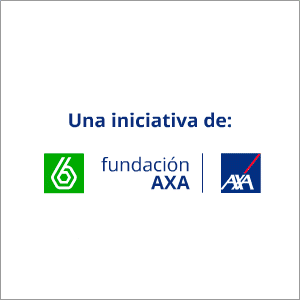
Existen enfermedades que están presentes ya desde el nacimiento. Son las que se conocen como congénitas. Aunque éstas pueden estar producidas durante el desarrollo embrionario o el parto, algunas son consecuencia de un defecto genético hereditario. Como si de un legado se tratara, este defecto se va heredando generación tras generación. Desde hace un tiempo es posible detener esta descendencia en algunas patologías con el diagnóstico genético preimplantacional (DGP). Es una técnica que combina la reproducción asistida y la genética molecular que permite estudiar el ADN de los embriones para seleccionar aquellos libres de anomalías cromosómicas y mutaciones genéticas. De esta manera, se consigue evitar la enfermedad y acabar con la transmisión familiar de ciertas patologías.
Sin embargo, ni todas las enfermedades son susceptibles de optar al DGP ni ética o legalmente es posible realizar esta selección de embriones en todos los casos. De entrada, la normativa establece que para poder optar al diagnóstico preimplantacional la enfermedad debe ser grave, de aparición precoz y no susceptible de tratamiento curativo postnatal. Los casos que no cumplen estos requisitos se evalúan de manera individualizada por parte de la Comisión Nacional de Reproducción Humana Asistida.
Es el caso, por ejemplo, del síndrome Brugada. Aunque esta enfermedad no se considera de aparición precoz y puede ser controlada tras el nacimiento, sus fatales consecuencias, como la muerte súbita, hacen que sea una candidata de estudio, apunta Anna Abulí, asesora genética de Salud de la Mujer Dexeus. El riesgo de transmitir la mutación es del 50%, aunque únicamente un 30% desarrollará la enfermedad. Ello se debe a que tiene una penetrancia incompleta, es decir, no todos los miembros que hayan heredado la mutación desarrollarán una muerte súbita. Pero, como apunta el cardiólogo Ramon Brugada, es muy difícil convencer a una madre que ha sobrevivido una muerte súbita de que aunque su hijo tenga la mutación no tiene por qué tener riesgo.
Por otro lado, a pesar de que ya se han identificado más de 200 mutaciones en ocho genes distintos, éstas no están presentes en todas las familias estudiadas, aclara Ramon Brugada. Ello indica que la enfermedad es heterogénea, es decir, que todavía quedan muchas otras mutaciones por descubrir y, por tanto, no en todos los casos puede realizarse DGP. Normalmente es el cardiólogo quien realiza el diagnóstico de síndrome Brugada.
Con el diagnóstico ya hecho, se hace un estudio genético para identificar la mutación, pero para recurrir a un diagnóstico genético preimplantacional el centro de reproducción asistida deberá pedir autorización previa al Departament de Salut de la Generalitat. Desde este organismo envían la información a la Comisión Nacional de Reproducción Humana Asistida, donde valorarán el caso.
La técnica se realiza mediante reproducción asistida. Tras la estimulación ovárica, se extraen los óvulos de la paciente y se realiza una inseminación con el esperma del hombre. Al tercer día de desarrollo, cuando los embriones tienen entre seis y diez células, se realiza una biopsia de los éstos. Extraemos una célula de cada embrión para descartar los que son portadores de la enfermedad. Si la célula es normal todo el embrión lo será y, por tanto, no es portador de la mutación, explica Mónica Parriego, coordinadora del programa de diagnóstico genético preimplantacionalde Salud de la Mujer Dexeus. En 48 horas se realiza el análisis de las células para determinar si los embriones son portadores. Los resultados se envían al laboratorio de fecundación in vitro, donde escogerán de uno a tres embriones libres de la patología y con
buen desarrollo para ser transferidos al útero materno. Puede ser que no encontremos ningún embrión sano o, al contrario, que todos lo sean. El factor edad también es muy importante ya que disponer de más embriones para el análisis implica mayor probabilidad de que alguno de ellos no esté afectado. En cualquier caso el proceso se puede repetir, señala Mónica Parriego. La tasa de embarazo puede ser, incluso, mayor que con la fecundación in vitro convencional ya que con frecuencia son parejas que no tienen problemas de fertilidad.