Nueva posible estrategia para reducir el colesterol malo
Se han cribado una colección de aproximadamente 130.000 compuestos y han encontrado una clase de moléculas que disminuían la secreción de apoB y reducían los niveles de colesterol.
Investigadores de la Universidad Médica de Carolina del Sur (Estados Unidos) han desarrollado un novedoso sistema para buscar nuevos compuestos terapéuticos que reduzcan la secreción de apolipoproteína B (apoB), el principal componente proteico de la partícula LDL, a partir de células hepáticas.
En su trabajo, publicado en la revista científica ´Communications Biology´, han cribado una colección de aproximadamente 130.000 compuestos y han encontrado una clase de moléculas que disminuían la secreción de apoB y reducían los niveles de colesterol. Estas moléculas tienen el potencial de ofrecer un nuevo régimen de tratamiento para pacientes con hipercolesterolemia familiar (HF).

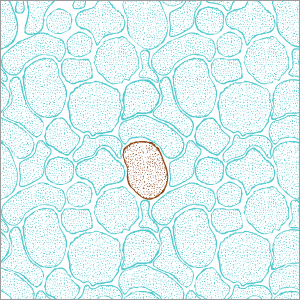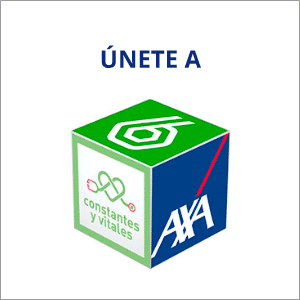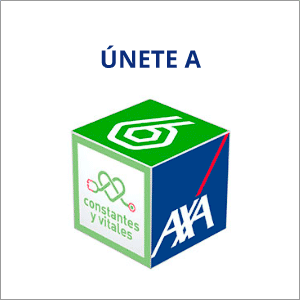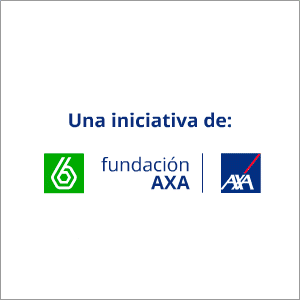
La HF es un trastorno genético que aumenta el riesgo de padecer enfermedades cardiovasculares, debido al aumento de los niveles de colesterol malo en la sangre. Normalmente, el receptor de lipoproteínas de baja densidad (LDLR) se une al colesterol circulante y lo lleva a las células hepáticas, donde se descompone.
Sin embargo, en la HF el LDLR está mutado, por lo que el hígado no puede eliminar tan bien el colesterol, lo que da lugar a una hipercolesterolemia. Según la Asociación Americana del Corazón, aproximadamente 1 de cada 200 adultos es portador de la mutación HF.
A los pacientes con colesterol alto se les suelen recetar estatinas. Las estatinas reducen el colesterol aumentando los niveles de LDLR; sin embargo, su eficacia varía mucho de una población a otra, y los pacientes con mutaciones homocigóticas en la HF son resistentes al tratamiento con estatinas porque su gen LDLR está mutado.
Para identificar posibles nuevas terapias, los investigadores crearon células similares al hígado humano a partir de células madre pluripotentes inducidas (iPSC). Las iPSC son células madre artificiales derivadas de células de la piel o de la sangre. Esta técnica permitió al equipo producir un gran número de células para analizar una amplia biblioteca de compuestos químicos. Utilizando este sistema modelo, el equipo descubrió una clase única de compuestos prometedores para el tratamiento de la HF. Descubrieron que los niveles de apoB disminuyen mucho cuando administramos el fármaco a las células. “Los niveles de colesterol bajan y también los de triglicéridos“.
A continuación, el equipo probó estos compuestos en un modelo preclínico de ratón. Sin embargo, sorprendentemente, estos compuestos resultaron ineficaces en el ratón. Un examen más detallado de las células hepáticas del ratón demostró que éstas eran resistentes a los compuestos, lo que pone de manifiesto una diferencia clave entre un modelo celular humano y un modelo de ratón.
Para superar este obstáculo, utilizaron ratones Avatar, es decir, ratones diseñados para desarrollar un hígado a partir de células humanas, en lugar de células de ratón.
Este modelo de ratón humanizado es una herramienta poderosa; la presencia del hígado derivado del ser humano recapitula el perfil lipídico observado en los pacientes y, por tanto, representa un modelo para probar nuevas terapias en un sistema complejo. Los compuestos identificados en el cribado de iPSC también fueron eficaces en este complejo modelo animal.
En resumen, crearon un potente sistema para modelar enfermedades complejas y probar nuevos compuestos terapéuticos. El equipo identificó una nueva clase de compuestos que reducen eficazmente el colesterol, los triglicéridos y la apoB. Y lo que es más importante, estos fármacos actúan independientemente de la vía del LDLR, a la que se dirigen las terapias tradicionales, y ofrecen una terapia novedosa para los pacientes con HF.
Aunque este trabajo es prometedor, aún queda trabajo por hacer. “Descubrir cuál es la diana del fármaco y mostrar su mecanismo de acción es absolutamente prioritario“, han comentado los autores.
Aprender cómo funciona el fármaco es un siguiente paso fundamental y podría identificar otras proteínas importantes a las que podrían dirigirse otros medicamentos. Otra cuestión clave es cómo interactúan estos compuestos con la terapia convencional, como las estatinas. La combinación de estos fármacos podría tener un potente efecto reductor del colesterol, al disminuir tanto el que se fabrica como el que circula por el organismo. M.T.T./ L.D.B. (SyM)